En este momento de la pandemia, donde vemos en el mundo cómo distintos intereses se ponen en juego al momento de decidir qué países y de qué manera entran en la carrera de contar con vacunas para su población, cobra enorme importancia la posibilidad de disponer de vacunas propias.
Esta situación ya la hemos visto en la pandemia del 2009 de la gripe por el virus de la Influenza, donde muchos países recién pudieron acceder a las vacunas un año después que la infección golpeó a la población, haciendo estragos. En ese momento tuvimos suerte porque el virus tenía una contagiosidad mucho menor (a la del SARS-CoV-2), porque enseguida se descubrió un antiviral y porque a los meses se disponía de una vacuna.
Sin embargo, y a pesar de creer haber aprendido la lección sobre “qué hay que hacer” y “qué no hacer”, la situación se repite.
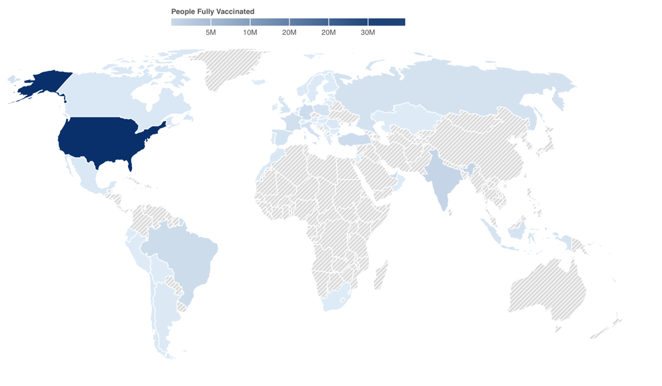
La OMS creó COVAX, una plataforma integrada por más de 100 países con el fin de evitar inequidades en la distribución de vacunas. No obstante, vemos que sólo 35 de los 193 países existentes hoy en nuestro planeta tienen acceso a vacunas para la Covid-19. Esto representa aproximadamente el 3% de la población mundial, y para alcanzar la inmunidad de rebaño se debe vacunar al 70-80% de esa pobación.
No hace falta alcanzar la inmunidad comunitaria o de rebaño para empezar a torcer el curso de la pandemia, dado que la vacunación también protege en forma individual. Pero la importancia de la inmunidad de rebaño radica en que nos permitirá alcanzar las condiciones sanitarias para sostener una situación controlada de transmisión del virus en una comunidad, en una región, en los países y en los distintos continentes.
A pesar de este dato, a priori desalentador, podemos decir que en dos meses de vacunación ya se ha inoculado a más personas que todas las que aparentemente se han infectado desde el comienzo de la pandemia.
Además, en estos primeros meses se han puesto en funcionamiento los sistemas de vacunación y también hemos experimentado los primeros, y esperables, incovenientes de producción y distribución de vacunas en el mundo. Esto debería servir para ajustar condiciones de trabajo y de preparación para el momento en que hayan más vacunas disponibles. Este cuello de botella era algo previsible, pero no pensábamos que iba a tener semejante impacto. El hecho de que ya estemos evidenciando el funcionamiento de las vacunas en la gran mayoría de los países ha generado una enorme expectativa en el mundo que nos lleva a ser muy optimistas, en el sentido de saber que con las vacunas es posible controlar el avance de la pandemia.
En nuestro país tenemos actualmente disponibles 3 tipos de vacunas: la Sputnik V (emplea vectores virales adenovirus con ADN para la proteína S del SARS-CoV-2), la de AstraZeneca/Oxford o Covishield (con vectores viral adenovirus de chimpancé ADN para la proteína S) y la de Sinopharm (emplea virus completo muerto).
Es importante disponer de vacunas distintas ya que se pueden aplicar, llegado el caso, a diferentes grupos poblacioneales si fuera necesario. Sin embargo, el número de vacunas y la velocidad de administración de las mismas no son suficientes. El segundo punto requiere de ajustes de condiciones locales de trabajo, algo totalmente manejable, mientras que el primero es mucho más complejo: depende de las negociaciones de las autoridades sanitarias nacionales con los titulares de las vacunas y de las condiciones de producción de las mismas.
El jueves 4 de marzo pasado se realizó en el Rectorado de la UNLP el lanzamiento formal del proyecto de diseño y producción de una vacuna para Covid-19. Este proyecto es el fruto de muchos años de estudio detrás de una vacuna que diseñamos junto al grupo del doctor Omar Azzaroni. Ambos grupos son de la Facultad de Ciencias Exactas.
El grupo del doctor Omar Azzaroni trabaja en el INIFTA (Instituto de Investigaciones Fisicoquímicas Teóricas y Aplicadas) dependiente de la UNLP y el Conicet, mientras que mi grupo trabaja en el IIFP (Instituto de Estudios Inmunológicos y Fisiopatológicos) dependiente de la UNLP y el Conicet y asocicado a la CIC (Comisión de Investigaciones Científicas de la Provincia de Buenos Aires).
Ciencia, instituciones y necesidades locales/regionales
Este proyecto es algo muy importante para nosotros porque se suma al trabajo que viene desarrollando el Grupo Covid Exactas desde marzo de 2020, y significa la posibilidad de que se pueda tener en el futuro próximo una vacuna de origen local. Además, con este proyecto pudimos demostrar el impacto que tiene el apoyo de las instituciones académicas y científicas en el desarrollo de necesidaes locales o regionales. De hecho, este proyecto complementa perfectamente el proyecto de la UNLP de contrucción de una planta de producción de vacunas, anunciado en diciembre de 2020.
Hablemos concretamente de este proyecto. Hemos diseñado una vacuna que estamos estudiando en ratones, es decir que estamos en la fase preclínica de investigación. Si bien no significa que contamos con una vacuna para aplicar en personas, es el paso previo obligado que todas las vacunas han debido atravesar para optimizar una que potencialmente podría emplearse en humanos.
En esta etapa estamos estudiando la seguridad (inducción de reacciones adversas luego de la administración) e inmunogenicidad (inducción de mecanismos inmunes). El próximo paso será optimizar el esquema de vacunación (cantidad de vacuna o dosis a administrar, frecuencia, intervalo de tiempo entre dosis, etcétera). Finalmente haremos los ensayos de protección en la etapa preclínica: vacunaremos a los ratones y luego los desafiaremos con el virus SARS-CoV-2 vivo para observar si estos animales se enferman o no en comparación a los animales que no reciben la vacuna, que deberían enfermarse en su totalidad. Recién en ese momento estaremos en condiciones de plantear la posibilidad de empezar un ensayo clínico fase 1 en humanos.
Cómo será la vacuna platense
La vacuna diseñada consiste en emplear proteínas del virus y un adyuvante (componente que potencia la activación del sistema inmune), que son nanopartículas orgánicas. Estas últimas son las que ha diseñado el grupo del doctor Omar Azzaroni con su equipo, y las hemos estudiado profundamente desde el 2018 en otros sistemas.
Para las proteínas del virus hemos trabajo con la colaboración de los grupos del doctor Sebastián Cavalitto del CINDEFI (Centro de Investigación y Desarrollo en Fermentaciones Industriales) y del doctor Javier Santos (Grupo Anticovid de la Facultad de Ciencias Exactas y Naturales de la UBA). Pero además estamos trabajando en colaboración con el doctor Alejandro Aiello del CIC (Centro de Investigaciones Cardiovasculares de la UNLP y Conicet) y su grupo, en los ensayos que nos permitirán estudiar si los anticuerpos que genera la vacuna tienen la capacidad de unirse a los virus y bloquear su entrada a las células.
Esta vacuna, como todas las que se encuentran en ensayos clínicos (aproximadamente 100), generan en el individuo vacunado la producción de anticuerpos bloqueantes dirigidos a la proteína S. Esta proteína se encuentra en la cubierta del virus y es la llave que le permite entrar a las células de nuestro organismo (principalmente células del pulmón y del intestino) a través de un receptor, ACE 2 o receptor de angiotensina 2, y de esa manera acceder al interior de las células para utilizar su maquinaria en provecho de la produccion de componentes virales y nuevos virus (ver figura).
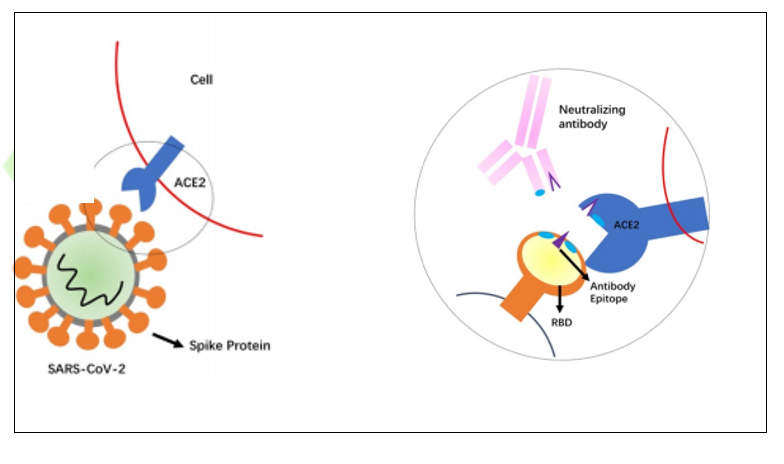
De esta manera, los virus se replican en el interior de nuestras células y salen a invadirlas. De no frenarse ese proceso, la enfermedad avanza y se producen las consecuencias clínicas conocidas.
Con esta vacuna, lo que se logra es que los anticuerpos bloqueantes producidos se unan a la proteína S y, de ese modo, se bloquee la invasión de las células y la generación de nuevas partículas virales.
Vacuna “con memoria”
Pero la vacuna no sólo genera anticuerpos, sino también células (lindocitos B y T) que son las que van a generar la memoria inmunológica. Esto permite que uno, luego de vacunado, esté preparado para futuros encuentros con el virus y estas células generen los anticuerpos en forma inmediata (2-3 días) para impedir su diseminación y la enfermedad.
Existen actualmente en fase 3 siete vacunas de este tipo en base al empleo de proteínas virales, lo cual refleja que esta estrategia ha sido planteada por otros grupos como algo potencialmente eficiente para controlar la infección viral. Por caso, la vacuna de Sinovac (China) se está aplicando en distintos países, entre ellos Chile y Brasil; la Bektop (otra vacuna de Rusia) se está empleando en Rusia; la Novavax (producida en Estados Unidos) se está estudiando en ese país, Inglatera y Sudáfrica, etcétera.
La importancia de contar con una vacuna de producción local tiene, como mencionamos anteriormente, varias ventajas.
En primer lugar, que la UNLP junto al Conicet y la CIC estén sosteniendo nuestro proyecto posiciona a estas instituciones de una manera especial en el contexto nacional, pero también en el local, con una importancia que refleja el trabajo conjunto que se está realizando.
En segundo lugar, la posibilidad de producir una vacuna localmente nos independizará del contexto mundial de producción y provisión de vacunas. Además, el hecho de poder diseñar una vacuna es relevante al momento de considerar lo que está ocurriendo con las nuevas cepas virales, algunas de las cuales han mostrado que no son bloqueadas por las vacunas actuales.
Entre ellas hay que considerar las variantes de Inglaterra o B.1.1.7, la de Sudáfrica o B.1.351 y la variante de Manaos o P1. Estas variantes, entre otras miles que han aparecido, se caracterizan porque presentan mutaciones o variaciones en la zona de la proteína S o Spike que alteran la capacidad de reconocimiento de su receptor, lo cual mejora el ingreso del virus a las células blanco. Esto determina, por ejemplo, que AstraZeneca/Oxford haya suspendido la vacunación en Sudáfrica porque la eficiencia de su vacuna se redujo a menos del 30%.
En este sentido, con nuestro grupo estamos en condiciones de generar proteínas S similares a las de las nuevas variantes, de manera que podremos producir una vacuna específica para administrar si la variante de Manaos, por ejemplo, se diseminara en nuestra población y las otras vacunas no fueran eficientes. Y lo mismo para cualquier otra variante que se detecte en nuestro medio.
Finalmente, es probable que la infección por SARS-CoV-2 se instale como una epidemia con ciclos anuales y se requieran vacunaciones estacionales, como es el caso de la gripe. Ante esa posibilidad debemos tener una provisión sostenida de vacunas, y lo mismo ocurrirá en todo el mundo, por lo que se estima que los problemas de producción y logística persistirán en el tiempo. En el mismo sentido, si aparecen nuevas variantes virales locales, la posibilidad de tener que hacer vacunaciones de refuerzo con vacunas dirigidas a las mismas es algo que estamos considerando.
En conclusión, creemos que la posibilidad de poder contar en un futuro con una vacuna local es algo sumamente importante y atractivo, no sólo desde lo académico y científico, sino que refleja el rol que tienen las instituciones académicas y científicas en nuestra sociedad, y en particular en nuestra región. Un país sin ciencia propia está condenado a la dependencia.


























































































